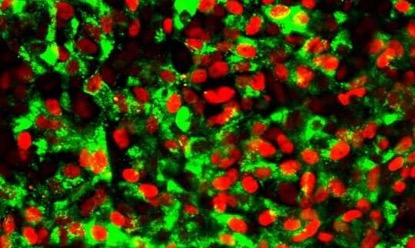
干细胞技术有望开发治疗糖尿病的细胞替代疗法
时间:2020-08-05
A-
A+
近日,一项刊登在国际杂志Nature Biotechnology上的研究报告中,来自德国环境健康研究中心等机构的科学家们通过研究开发了一种改进型的多能干细胞分化技术,其能在体外产生具有良好葡萄糖反应和胰岛素分泌的细胞,而这是迈向细胞替代疗法的重要一步。
自身免疫性损伤所诱发的分泌胰岛素的β细胞的缺失会导致1型糖尿病发生,临床上胰岛细胞的移植或能潜在治疗糖尿病,但供体的胰腺却非常稀少;近日,一项刊登在国际杂志Nature Biotechnology上的研究报告中,来自德国环境健康研究中心等机构的科学家们通过研究开发了一种改进型的多能干细胞分化技术,其能在体外产生具有良好葡萄糖反应和胰岛素分泌的细胞,而这是迈向细胞替代疗法的重要一步。
图片来源:©Helmholtz Zentrum München
人类多能干细胞(人类胚胎干细胞和诱导多能干细胞)能够分化成为任何一种具有自我更新能力的细胞类型,因此多能干细胞就是产生特殊细胞类型用于细胞替代疗法的最佳来源,比如产生用于治疗糖尿病患者的β细胞,然而由于存在较多的分化步骤,目前体外β细胞的分化过程比较复杂,这一过程需要几乎20种信号蛋白和小型分子来调节细胞的生长和分化,而且能够持续超过四周时间。在这个多步骤过程中,并不是所有的细胞都能分化为靶向性细胞,其会采用错误的分化途径,这就会导致高度异质性的β细胞群体产生,而其并不具备完全的细胞功能,因此,研究人员就想通过研究改善干细胞衍生的β细胞的质量。
随后研究人员开发了一种方法,其能利用高度特异性的胰腺祖细胞来丰富干细胞的培养,这就能促进干细胞更有针对性地分化为β细胞;研究者Heiko Lickert教授说道,从发育生物学的角度来看,我们知道胰腺祖细胞在分化第一步的内胚层阶段已经被指定,因此我们就需要弄清楚这是否也适用于人类多能干细胞的分化,随后研究人员开始分析如何更好地控制内胚层的质量以及其如何分化为特异性的胰腺祖细胞,通过联合研究后,研究人员识别出了一种名为CD177的单克隆抗体,其能标记内胚层亚群,从而就能时期有效并均匀地分化为特定的胰腺祖细胞;CD177能扮演质量控制者的角色,在其帮助下,研究人员就能在早期观察到细胞是否会处于争取的分化轨道上,这样就能节省大量的时间、精力和金钱。
在内胚层阶段利用CD177来丰富干细胞培养液或能增加特异性胰腺祖细胞的产生,最终就会导致更多成熟功能且能对葡萄糖有效反应的β细胞产生,同时还能改善机体胰岛素分泌的模式;当前的β细胞分化步骤能够产生异质性的细胞群体,其不仅含有β细胞,还含有来自不同细胞谱系的残留胰腺祖细胞或其它细胞类型,通过CD177的纯化不仅能够改善所产生的β细胞的异质性和质量,还能增加其临床安全性,而这是迈向1型糖尿病患者干细胞衍生的β细胞替代疗法转化的关键一步。此外,由于基于CD177所产生的β细胞与人体内的β细胞较为相似,因此CD177步骤或能帮助建立模拟人类胰腺的疾病模型系统,这种新型的分化步骤或能帮助研究者产生功能性的β细胞从而用于药物筛选和新型疗法的开发。总体来看,间充质干细胞治疗具有良好的安全性记录,对病人无明显毒副作用,少数病人出现注射局部不适、短暂低热等,对症处理即可。
一人存储,全家受益:干细胞用于异体时不需要配型,存储干细胞,当任何一个家人有需求时,都可以使用,让全家人都多了一份保障。
目前临床采用的干细胞主要是来自异体的间充质干细胞,不过随着技术的不断进步,越来越多的人认可采用自体干细胞进行治疗,这就需要提前进行储存,目前我们了解的干细胞储存主要是胎盘及脐带血等围产期干细胞储存,而现在牙髓间充质干细胞的储存也越来越普及。
原始出处:
文章来源生物谷
Mahaddalkar, P.U., Scheibner, K., Pfluger, S. et al. Generation of pancreatic β cells from CD177+ anterior definitive endoderm. Nat Biotechnol (2020). doi:10.1038/s41587-020-0492-5