人类胚胎干细胞正重塑生物学概念
时间:2018-05-08
A-
A+
此类研究促成了可能是本世纪再生医学和生物学研究领域最大的创新:诱导多能干(iPS)细胞的发现。2006年,日本京都大学干细胞生物学家Shinya Yamanaka仅利用4个遗传因子,成功地使成年小鼠细胞返回到像胚胎一样的状态。次年,他和Thomson在人类细胞中实现了同样的壮举。理论上,这一过程提供了和治疗性克隆相同的潜在回报——无限量供应同患者基因匹配的多能细胞,但不会出现道德困境。
1998年,当研究人员最早弄清楚如何获得人类胚胎干细胞时,Dieter Egli正要开始念研究生。自此以后的20年里,这种多产细胞一直伴随着Egli的职业生涯。这位如今在美国哥伦比亚大学工作的生物学家,利用它们探寻了来自成人细胞的DNA如何被重新编程成胚胎状态,并且解决了关于糖尿病发生和治疗的问题。Egli甚至帮助开发了一种全新的人类胚胎干细胞形式。其能简化关于不同人类基因做了什么的研究。
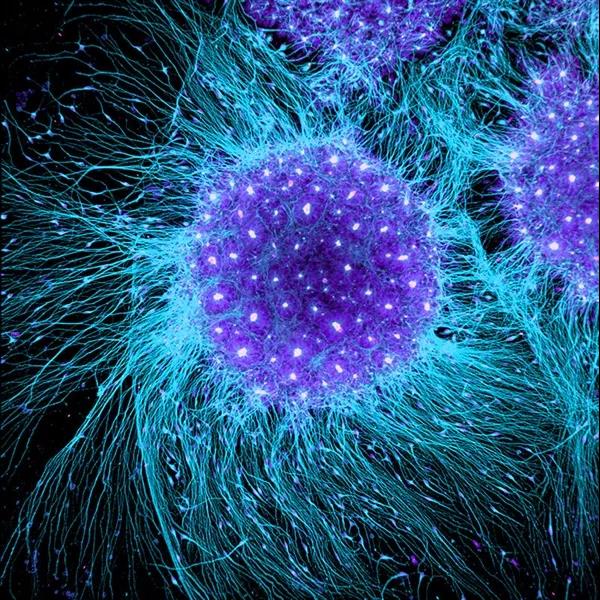
来自人类胚胎干细胞的神经“花结”组装成正在培养的球体。
图片来源:Gist Croft/Ali Brivanlou/Rockefeller University
广泛的研究让Egli成为胚胎干细胞生物学领域的领军者。该领域面临着资助受限以及狂热追寻竞争技术的挑战。尤其是各种同类技术,并未带有相同的伦理标准。不过,很多人认为,如今人类胚胎干细胞变得比以往任何时候都重要。“对于胚胎干细胞,我感到非常兴奋。”Egli说,“它们将带来改变生活的史无前例的发现。对此,我毫不怀疑。”
胚胎干(ES)细胞提供了关于早期发育的优质信息。正如天文学家回顾宇宙大爆炸以寻求关于宇宙的基本见解,生物学家探究这些细胞内的分子以寻找关于单个原始细胞如何变成几万亿个细胞并且拥有一系列令人眼花缭乱的形式和功能的线索。科学家学会了如何将这种细胞变成几十种代表身体内各种组织和器官的成熟细胞。从2010年试图修复脊髓损伤的努力开始,已有十几项利用ES细胞创建的细胞开展的临床试验,旨在治疗帕金森氏症、糖尿病和其他疾病。早期结果表明,一些方法正在奏效:一份日前发布的期待已久的报告证实,两名患有同年龄相关的黄斑变性的病人在视力上出现了改善。黄斑变性是一种破坏视觉敏锐度的疾病。
试探性的开端
1981年,研究人员成功培养出来自小鼠胚胎的干细胞。他们很快意识到这项发现的巨大潜力,因为这些细胞既能自我复制,又可被推动变成身体200余种细胞类型中的任何一种。不过,此项技术并不容易在灵长类动物身上实现。威斯康辛大学麦迪逊分校生物学家James Thomson花了14年时间,才将该技术成功用于猴子。3年后,Thomson利用生育治疗中未使用的捐赠胚胎,创建了全球首个人类ES细胞系。
此项发现激起了一场道德风暴。批评者——大多数来自宗教界——认为胚胎构成了人类的一部分,并且想阻止任何涉及破坏胚胎的研究。2001年,美国总统乔治·沃克·布什将政府资助限制在仅针对一些现有ES细胞系的研究上。此项决定迫使那些打算在该国开展相关研究的科学家寻求私人或者各州资助,并且经常创建两个实验室—— 一个针对ES细胞研究,另一个开展由美国联邦政府资助的工作。在包括德国和意大利在内的其他国家,创建此类细胞则被完全禁止。
不过,相关研究还是在能够开展的地方继续进行。澳大利亚、新加坡、以色列、加拿大、美国以及一些其他国家的研究人员很快报告称,他们将胚胎干细胞转化成神经元、免疫细胞和跳动的心脏细胞。
此类研究促成了可能是本世纪再生医学和生物学研究领域最大的创新:诱导多能干(iPS)细胞的发现。2006年,日本京都大学干细胞生物学家Shinya Yamanaka仅利用4个遗传因子,成功地使成年小鼠细胞返回到像胚胎一样的状态。次年,他和Thomson在人类细胞中实现了同样的壮举。理论上,这一过程提供了和治疗性克隆相同的潜在回报——无限量供应同患者基因匹配的多能细胞,但不会出现道德困境。
为研究遗传病带来新工具
研究人员还在尝试生长器官。如果获得正确的信号分子和3D环境,ES细胞可组成被称为类器官的复杂组织,即便是在培养皿中。这种能力对于诸如俄亥俄州辛辛那提儿童医院的James Wells等研究人员来说非常重要。Wells正在培养肠道类器官,以便用于测试药物,并且可能有一天用于器官移植。
同时,ES细胞的新来源为研究遗传性疾病带来了新工具。例如,2004年,芝加哥的生殖科医生开始利用通过体外授精创建的胚胎产生ES细胞系。这些胚胎被发现有遗传缺陷,因此无法被用于不孕治疗。这项努力使该团队创建了地中海贫血症、亨廷顿氏病、马凡综合征、肌肉萎缩症和其他遗传疾病的分子模型。2007年,研究人员利用ES细胞阐明了导致在被称为脆性X综合征的可遗传疾病中见到的认知损伤的分子变化。
研究人员表示,iPS细胞为在培养皿中研究疾病带来了更多前景——可利用任何患有疑似遗传疾病的活着的人生长出干细胞。不过,很多人仍看到了ES细胞在该领域的巨大潜力。ES细胞仍能起到辅助作用。
例如,2008年,来自哈佛大学的Kevin Eggan产生了来自神经退行性疾病——肌萎缩性脊髓侧索硬化(ALS)患者的iPS细胞系。Eggan从此前利用ES细胞开展的工作中了解到如何“诱骗”多潜能细胞变成受ALS影响的大脑细胞——运动神经元。当利用来自患者的iPS细胞开展相同工作时,他能迅速地比较两类细胞。和未患有ALS的人相比,来自患者的细胞放出更多电。“我们利用了用ES细胞开展的所有工作来了解运动神经元。”Eggan表示。如今,一种令来自患者的iPS细胞沉默的抗癫痫药物正在人类身上测试。结果有望在两个月后出炉。
重要性一如从前
ES细胞研究仍有上升的空间,如果能跨过一些障碍的话。一个大问题是产生很多细胞类型极具挑战性。据Melton估测,迄今为止,仅有10种左右的细胞可真正在功能上向普通的人类细胞看齐。同时,一些有着最深远用途的细胞,比如卵子和精子,在可预见的未来仍将是一个挑战。
该领域还面临着资助上的不确定性。科学家频频听到美国总统唐纳德·特朗普可能对关于ES细胞研究的联邦资助实施新限制的传闻。不过,很多研究人员认为,尽管有着跌宕起伏的历史,但ES细胞一再通过一些难以预测的方式证实了它们的价值。一些人甚至相应减少了对动物模型的使用,因为ES细胞似乎提供了研究人类疾病的更好路径。
Yamanaka表示,ES细胞推动了其关于iPS细胞的研究工作。同时,是Thomson针对人类ES细胞的“处方”,使从小鼠转向人类iPS细胞的努力仅在1年内便得以实现。而此前,从小鼠到人类各种ES细胞的转变用了近20年。“我们确切地知道应当如何培养人类iPS细胞。”Yamanaka说。
他认为,ES细胞对于理解多能性机制和改善任何多能细胞的医疗用途同样至关重要。“现在,人类ES细胞的重要性不亚于20年前。我想象不到未来它的重要性将会变低。”